Voda (H2O) ali sistematično oksidan je anorganska spojina, katere molekule vsebujejo en kisikov in dva vodikova atoma, povezana s kisikom s kovalentno vezjo. Kot med vodikovima atomoma meri 104,45°. Je najenostavnejši vodikov halkogenid in daleč najbolj preučevana kemijska spojina. Naziv "voda" se običajno uporablja za vodo v tekočem agregatnem stanju pri standardni temperaturi in tlaku. V naravi se pojavlja v več agregatnih stanjih: v tekočem stanju v ozračju tvori dež in meglo, oblaki so sestavljeni iz suspendiranih kapljic vode in ledu, kristaliziran led pa lahko pade na zemljo kot sneg.
Anomalno Širjenje Vode pri Zmrzovanju
Ena izmed najbolj izjemnih in kritičnih lastnosti vode je, da se njena gostota pri zamrzovanju zmanjša. To pomeni, da led zavzema pri isti masi večjo prostornino kot tekoča voda. Poleg bizmuta, silicija, germanija in galija je voda redka snov, ki izkazuje to anomalno obnašanje. Poskusi so pokazali, da se, ko 1 m³ vode tvori led, njena prostornina poveča na približno 1,11 m³.
Fizikalno Ozadje Anomalije
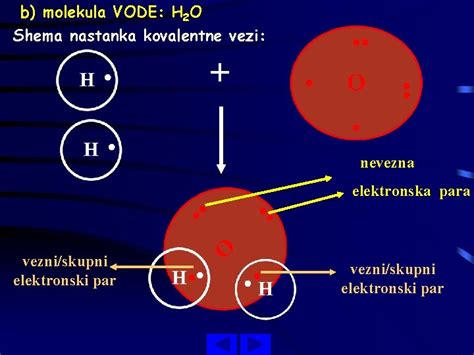
Anomalija je posledica posebne strukture molekule vode in močnih vodikovih vezi. V molekuli vode tvorita vodikova atoma s kisikovim atomom kot 104,45°. Vodikova atoma sta blizu dveh oglišč tetraedra s kisikovim atomom v središču, v drugih dveh ogliščih pa sta elektronska para valenčnih elektronov, ki ne sodelujeta v tvorbi vezi. Ker je kisik bolj elektronegativen kot večina drugih elementov, svoje elektrone obdrži, medtem ko sta vodikova atoma pozitivno nabita, kar daje molekuli vode polarnost.
Molekula vode lahko zaradi svoje polarnosti v tekočem in trdnem stanju tvori štiri vodikove vezi s sosednjimi molekulami vode. Vodikova vez je približno desetkrat močnejša od Van der Waalsove sile, ki privlači molekule v večini tekočin. Te vodikove vezi so vzrok za anomalne lastnosti, ki vodi določajo lastnosti in omogočajo življenje. Pri zniževanju temperature z 4 °C na 0 °C se molekule vode prerazporedijo v nenavadno, bolj odprto tridimenzionalno strukturo ledu, ki pušča veliko "praznin" in s tem zmanjša gostoto.
Posledice Širjenja v Naravi in Gospodinjstvu
Povečanje volumna vode pri zamrzovanju ima daljnosežne posledice tako v naravi kot v vsakdanjem življenju:
- Pokanje materialov: Zadošča, da postavite polno plastenko vode v zamrzovalnik; po nekaj urah bo voda zmrznila in plastenka bo počila, kar potrjuje pojav širjenja. Enako se dogaja z vodovodnimi cevmi in drugimi posodami. Pozimi pogosto pokajo tudi avtomobilski radiatorji, če vanje ni bil dodan antifriz.
- Geološko preperevanje: V naravi širjenje ledu povzroča razrivanje materiala in pokanje skal, kar je pomemben dejavnik pri fizikalnem preperevanju.
- Plavanje ledu: Izjemno pomembna posledica je, da led na vodi plava. V jezerih in oceanih se voda z najvišjo gostoto pri 4 °C potopi na dno, led pa plava na tekoči vodi in tvori ledeno skorjo. Led kot toplotni izolator preprečuje prehitro ohlajanje vode proti dnu in zamrzovanje celotnega vodnega telesa, kar je ključnega pomena za preživetje vodnih organizmov pozimi. Približno 9 % ledene gmote gleda iz vode, večina ledu pa je pod vodo.
- Poškodbe konstrukcij: Ko voda vstopi v pore ali razpoke kamna, kot so granitne ploščice, in zmrzne, se njena prostornina poveča. Če je sila raztezanja ledu večja od konstrukcijske sile kamna, se kamen zlomi. S ponavljanjem ciklov zamrzovanja in odmrzovanja se razpoke širijo, kar sčasoma vodi do razbitin.

Fizikalne Lastnosti Vode in Ledu
Tališče in Vrelišče
Pri tlaku 1 atm se led tali ali voda zmrzuje pri 0 °C. Pri enakem tlaku voda vre ali para kondenzira pri 100 °C. Voda lahko prehaja v plinasto fazo tudi pri nižjih temperaturah z izhlapevanjem na površini (vretje je definirano kot izparevanje po celem volumnu). Tališče in vrelišče sta odvisna od tlaka. V večini snovi se njihov volumen med taljenjem povečuje, zato temperatura tališča z naraščajočim tlakom narašča. Pri vodi pa se volumen pri taljenju zmanjšuje, zato tališče z naraščajočim tlakom pada. Na morski gladini je vrelišče vode 100 °C, z naraščajočo nadmorsko višino pa zračni tlak pada, zato pada tudi temperatura vrelišča: za 1 °C vsakih 274 metrov.
Vodikove Vezi in Specifična Toplota
Vodikove vezi so vzrok tudi za izjemno visoko specifično toploto vode (okoli 4,2 J/g/K), talilno toploto (okoli 333 J/g) in izparilno toploto (2257 J/g). Te lastnosti povzročajo, da je voda najučinkovitejši regulator podnebja na Zemlji, saj shranjuje in prenaša ogromne količine energije med oceani in ozračjem. Energija vodikove vezi vode je okoli 23 kJ/mol, kar je približno dvajsetkrat šibkeje od kovalentne vezi O-H (492 kJ/mol).
Matematični Model Zamrzovanja Kapljic
Geometrijski opis zamrzovanja kapljice je kompleksen, zato se za razumevanje pojava singularnosti pri zamrznitvi kapljic pogosto uporablja poenostavljen model. Namesto realne oblike kapljice, ki je odvisna od zunanjih pogojev, se predpostavi, da ima kapljica na začetku obliko odrezane krogle. Proces zamrzovanja in premikanje mejne ploskve med trdno in tekočo fazo vode se poenostavi tako, da je mejna ploskev med ledom in vodo ravna in vzporedna s podlago ter se pri dviganju prilagaja začetni obliki kapljice, ne da bi se širila v radialni smeri.
Gostotni Količnik in Oblika Ledenih Kapljic
Med procesom zmrzovanja se masa vode ohranja. Zato se z večanjem mase ledu zmanjšuje masa vode v kapljevinastem stanju. Pri tem se vpelje parameter ν, gostotni količnik, ki je enak razmerju gostot vode v trdnem (ρs) in kapljevinastem (ρl) agregatnem stanju (ν = ρs/ρl). Model pokaže, da ta količnik ključno vpliva na končno obliko zamrznjene kapljice.
Numerične rešitve modela ledenih kapljic prikazujejo različne oblike glede na gostotni količnik: čim manjši je gostotni količnik, tem bolj špičast je vrh kapljice, ko ta v celoti zmrzne. Za količnike, večje od kritične vrednosti (νc), ostane vrh kapljice zaobljen. Numerični model tvori špico pri gostotnem količniku, ki je enak ali manjši od ν = 3/4. Oblika špice ni odvisna od kota s podlago, ne glede na gostotni količnik ν.
Dinamika Rasti Kristalov in Hitrost Zmrzovanja
Ko vodna kapljica v celoti zmrzne, pogosto tvori oster koničast vrh, kjer se začnejo nabirati kristalčki in sčasoma pokrijejo celotno ledeno kapljico. Rast kristalov je najhitrejša na delih, kjer je največja difuzija vodne pare, torej na ostrih konicah, kjer se ustvari velik gradient koncentracije vodne pare. Teorija difuzijsko omejene agregacije, ki sta jo vpeljala fizika T.A. Witten in L.M. Sanders, je pomembna za razumevanje dinamike snežink in rasti kristalov, kjer so ključni deli kristala z majhnim krivinskim radijem.
Hitrost širjenja ledene plasti je odvisna tudi od kontaknega kota kapljice s podlago. Čim večji je kontaktni kot, daljši je čas zmrzovanja, saj je pri enaki količini vode kapljica višja. Zanimivo je, da je rast kristalčkov na površini kapljice, ki je zmrznila na hidrofobni podlagi, hitrejša.
3D molekularna vizualizacija - Voda se spreminja v led
Praktični Vidiki Zamrzovanja Vode
Zamrzovanje Vodovodnih Cevi in Poškodbe
Zaradi širjenja vode ob zamrzovanju so vodovodne cevi izpostavljene velikim tveganjem. Cev ne poči med odtajanjem, temveč takrat, ko voda v njej zmrzuje. Če je voda v cevi, še posebej, ko sta oba konca zamrznjena ali je dovod k zaprti pipi zamrznjen, popolnoma zaprta, se njen volumen ob zmrzovanju poveča. Cev se mora raztegniti; če ni dovolj elastična (npr. pocinkane cevi, kjer poči koleno ali T-komad iz bele litine), poči. Jeklena cev se lahko plastično deformira in po odtalitvi zadrži povečan premer, vendar se bo ob ponavljajočem zamrzovanju in tajanju tudi ta sčasoma zlomila.
Zaščita pred Zamrzovanjem
Za preprečevanje zamrzovanja je ključna zaščita površine vodovodnih cevi, zlasti zunanjih, z uporabo toplotnoizolacijskih materialov, kot so tople cevi, bombaž ali konoplja. Pri gradnji objektov morajo biti temelji načrtovani tako, da je globina temeljenja (Hf) enaka ali večja od največje globine, do katere prodre zmrzal v prostem terenu (H0), znane kot globina zmrzovanja. Ta se določa z izračunom indeksa zmrzovanja (ali indeksa mraza) za določeno obdobje.
Metode Odmrzovanja Cevi
Kadar cevi že zamrznejo, se lahko poslužujemo več metod odmrzovanja:
- Kapljanje vode: Odprtje pipe za sanitarno vodo do te mere, da voda teče po kapljici, preprečuje zamrzovanje, saj tekoča voda ne zmrzne, tudi pri nizkih temperaturah. To je učinkovita preventivna metoda v mrzlem vremenu.
- Odmrzovanje z vročo vodo in brisačo: Zamrznjeno pipo in cev pokrijemo z vročo brisačo ali vlažno krpo, nato pa počasi in postopoma nalivamo vročo vodo v cev. Neposredno nalivanje vrele vode v zmrznjene cevi, še posebej kovinske, ni priporočljivo, saj lahko povzroči pokanje zaradi hitre temperaturne spremembe.
- Odmrzovanje s sušilnikom za lase: Za cevi iz PPR materiala se lahko uporabi sušilnik za lase, ki s toplim zrakom postopoma tali led.
- Uporaba soli ali alkohola: Pri nedostopnih ceveh je mogoče vodo izsesati in nato v cev nasuti sol ter nanjo natočiti vrelo vodo. Sol zniža tališče ledu in pospeši taljenje. Podobno se lahko uporabi alkohol, ki je manj agresiven do cevi, vendar ga je treba ponavljati zaradi redčenja. Pri uporabi teh snovi je nujno zagotoviti, da ne pridejo v stik z živino ali pitno vodo.
- Električno taljenje (z varilnim aparatom): To metodo uporabljajo mojstri za taljenje ledu v kovinskih ceveh. Priklop varilnega aparata na dva konca cevi s ciljem segrevanja zahteva nizko upornost cevi in ustrezno visoko tokovno moč. Če je upornost previsoka (nizki tok), je segrevanje neučinkovito.

Zamrzovanje Slane Vode in Njihova Uporaba
Morska voda, ki v povprečju vsebuje okoli 3,5 % natrijevega klorida, se od sladke vode razlikuje po fizikalnih lastnostih. Zmrzne pri nižji temperaturi (okoli −1.9 °C), njena gostota pa s padajočo temperaturo narašča in svoje maksimalne vrednosti ne doseže nad lediščem, kot to velja za sladko vodo. Slanost morske vode se sicer spreminja, od okoli 0,7 % v Baltiku do 4 % v Rdečem morju.
Zmrznjena slana voda, vključno z morsko vodo, zmrzne in se tudi odtaja pri nekaj stopinjah nižje temperature kot sladka voda. To pomeni, da lahko zamrznjena slana voda v hladilni torbi vzdržuje nižjo temperaturo dlje časa kot zamrznjena sladka voda. To je uporabno za shranjevanje zmrznjenih živil, kot je sladoled, ki zahtevajo temperaturo pod 0 °C. Vendar pa zamrznjene slane vode ne moremo uporabiti kot rezervno pitno vodo. Za hlajenje pijač in sadja, kjer zadostuje temperatura okoli 0 °C, pa je sladka voda povsem primerna in nižja temperatura niti ni zaželena.
Druge Nevarnosti in Posebnosti
Poleg pokanja cevi zaradi širjenja ledu, so znani tudi primeri poškodb zaradi zmrzovanja v bojlerjih. Ko voda v bojlerju zamrzne in se grelec vklopi, se tanka plast ledu ob grelcu hitro stopi. Voda ima manjši volumen in steče navzdol, medtem ko grelec na vrhu ni več obdan z vodo, se hitro pregreje, zavre nekaj vode in paro pregreje. Para dobi hitro visok pritisk, kar lahko privede do razpočenja bojlerja, ne zaradi neposrednega širjenja ledu, temveč zaradi lokalnega pregrevanja in tlaka pare.
tags: #volumen #zamrznjene #vode

